【万化-新闻资讯】多国集体发声谴责以色列官员嘲讽被...2026-05-22
【万化-新闻资讯】习近平为普京举行欢迎仪式 现场奏...2026-05-21
【万化-新闻资讯】俄罗斯总统普京抵达北京 开启对华...2026-05-20
【万化-新闻资讯】消息人士称美方对伊朗开出5个关键...2026-05-19
【万化-新闻资讯】广西柳州发生5.2级地震 已致3...2026-05-18
【万化-新闻资讯】特朗普乘专机离京 中国军人现场英...2026-05-16
在化学世界中,大部分反应需要克服一个“能量障碍”——活化能。这就像两个人需要翻过一座高山才能相见。催化剂的作用就是为反应物提供一条翻山的捷径,大幅降低所需的能量门槛。
这个过程中,催化剂展现出三大特征:不改变化学平衡(不会改变“最终能走到一起的情侣”数量),不改变反应焓变(不改变这段“感情”的本质能量),以及最关键的——反应前后自身的质量和化学性质保持不变。
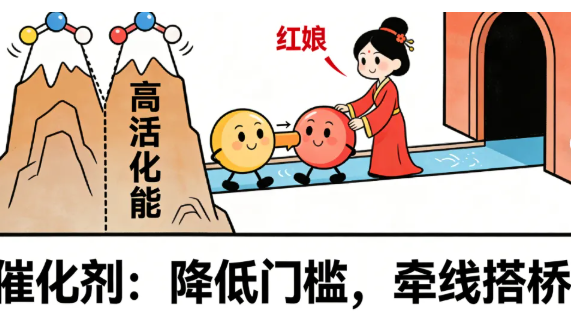
其核心原理可归纳为改变反应路径,降低反应所需的活化能。
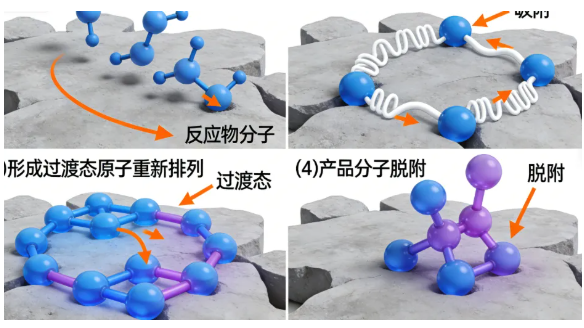
以最常见的异相催化为例,催化剂通常提供固体表面作为“相亲平台”,反应物分子被吸附在催化剂表面,化学键被削弱,分子结构发生形变,从而更容易发生反应。产物生成后,会从催化剂表面脱附,留下空位给新的反应物。
在化工领域,哈伯-博斯法合成氨(使用铁催化剂)被誉为“从空气中制造面包”的技术,生产的氮肥养活了全球约一半人口;石油裂化(使用沸石催化剂)将重质油转化为汽油、柴油等轻质燃料;合成高分子材料(如聚乙烯、聚丙烯)也离不开齐格勒-纳塔催化剂。
在环保领域,汽车三元催化转化器(使用铂、钯、铑等贵金属)可将尾气中的CO、NOx和未燃尽烃类转化为无害的CO₂、N₂和H₂O。
⚠️ 重要安全提示: 本文旨在科普化学原理。请勿在家尝试!
*免责声明:本公众号所载内容仅供参考之用,读者不应单纯接受公众号信息而取代自身独立判断,应自主做出决策并自行承担风险。本公众号不对任何因使用本公众号所载内容所引致的损失承担任何风险。⚠️非专业建议:本文内容不构成任何化学、医疗或健康建议。如您有任何相关问题,请咨询相关领域的专业人士。